Характеристика наностержней из золота (Au) в ближней инфракрасной области с помощью гиперспектральной микроскопии
Создание наностержней из золота (Au) со свойствами поглощения света во втором ближнем инфракрасном окне или коротковолновом инфракрасном диапазоне (SWIR) имеет большой потенциал для применения в тераностике. Длины волн SWIR обычно лежат в диапазоне 1000-1700 нм.
Основной областью применения оптически активных наностержней в SWIR-области является фототермическая терапия. При такой терапии лазерное излучение NIR во втором инфракрасном окне направляется на ткани, содержащие наностержни. При этом происходит нагрев локализованных Au-стержней и уничтожение опухолевых тканей в местах их расположения, а окружающие здоровые ткани остаются неповрежденными. Использование SWIR-наностержней позволяет применять лазеры с большей длиной волны, которые глубже проникают в ткань и значительно повышают эффективность фототермотерапии опухолевой ткани.
Эффективная разработка SWIR-наностержней для фототермотерапии требует правильного синтеза стержней с правильным аспектным соотношением (длина и диаметр), чтобы они были оптически активны в SWIR-диапазоне длин волн. Кроме того, они должны иметь соответствующий целевой белок для преимущественной колокализации с целевыми участками ткани. Эти вопросы разработки часто проверяются и демонстрируются с помощью усовершенствованной темнопольной гиперспектральной микроскопии компании CytoViva. Система CytoViva предназначена для оптической визуаизации и спектральной характеристики Au-наностержней в области SWIR. Система также может быть использована для подтверждения поглощения Au-наностержней в опухолевой ткани. Для получения таких изображений и данных в системе CytoViva используется запатентованная усовершенствованная оптика микроскопа темного поля, спектрофотометр с дифракционной решеткой и InGaAs камера для SWIR области. Для проверки спектрального отклика наночастиц и других важных критериев образца используется эффективное программное обеспечение для анализа гиперспектральных изображений.
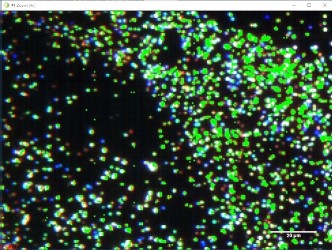
На рис. 1 представлено улучшенное гиперспектральное изображение в темном поле Au-наностержней с соотношением сторон, дающее SWIR-спектр.

Рисунок 1 – Наностержни Au, оптически активные в SWIR-области
Большинство этих Au-наностержней дают спектральный отклик при длине волны 1500 нм, как показано на рис. 3. Это можно подтвердить с помощью алгоритма классификатора пиковых длин волн в программе анализа гиперспектральных изображений, который сопоставляет каждый пиксель изображения со спектральным откликом на длине волны 1500 нм, как показано на рис. 2. На рис. 4 представлен отчет о распределении классов, иллюстрирующий количество пикселей, отображаемых для данного диапазона длин волн на 1500 нм.
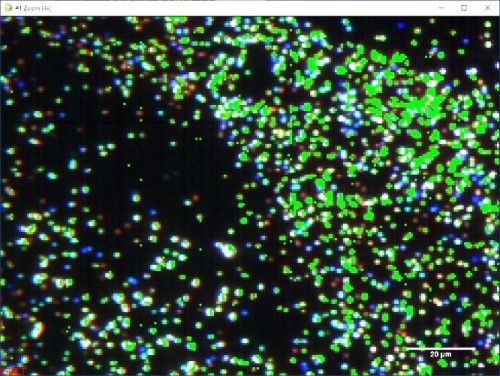
Рисунок 2 – Спектральное отображение (зеленый цвет) всех Au-наностержней с при 1500 нм
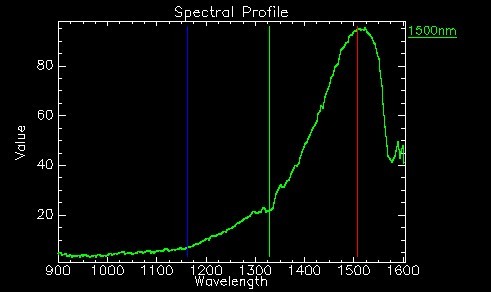
Рисунок 3 – Спектр при 1500 нм Au-наностержней, отображенных на рисунке 2
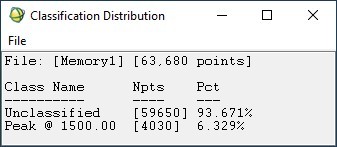
Рисунок 4 – Классовое распределение пикселей, отображающих спектр при 1500 нм на изображении
Для подтверждения поглощения Au-наностержней в целевых тканях образцы тканей, подвергшиеся воздействию Au-наностержней, могут быть визуализированы с помощью той же установки микроскопа. На рис. 5 показан неокрашенный образец ткани с интернализованными наностержнями.

Рисунок 5 – Усиленное гиперспектральное изображение наностержней Au в неокрашенной ткани, полученное с помощью гиперспектрального микроскопа в темном поле
На рис. 6 показано отображение наностержней с помощью алгоритма spectral angle mapper в программном обеспечении для гиперспектрального анализа. Этот алгоритм ищет совпадение полного оптического спектра наностержней на основе библиотеки спектров, которая была отфильтрована по отрицательному контрольному образцу ткани, что гарантирует отсутствие ложноположительного отображения.
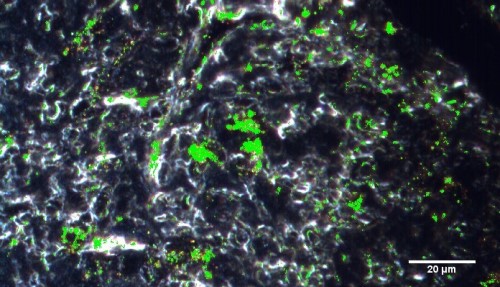
Рисунок 6 – Спектральное отображение Au-наностержней в ткани
Эти два примера иллюстрируют, как гиперспектральная SWIR-микроскопия CytoViva может быть использована для подтверждения правильности синтеза и функционализации SWIR-наностержней. Кроме того, она позволяет подтвердить тканевую локализацию целевых Au-наностержней. Эти возможности делают ее критически важным инструментом для эффективной разработки методик фототермотерапии.